
Estrutura de alcanos lineares, propriedades, nomenclatura, exemplos
O alcanos lineares são hidrocarbonetos saturados cuja fórmula química geral é n-CnH2n + 2. Por serem hidrocarbonetos saturados, todas as suas ligações são simples (C-H) e são compostas apenas por átomos de carbono e hidrogênio. Eles também são chamados de parafinas, diferenciando-os dos alcanos ramificados, que são chamados de isoparafinas..
Esses hidrocarbonetos não têm ramificações e anéis. Mais do que linhas, esta família de compostos orgânicos é mais parecida com cadeias (alcano de cadeia reta); ou do ponto de vista culinário, ao espaguete (cru e cozido).

O espaguete cru passa a representar o estado ideal e isolado dos alcanos lineares, embora com uma tendência pronunciada de quebrar; enquanto os cozidos, independentemente de estarem al dente ou não, aproximam-se de seu estado natural e sinérgico: alguns interagindo com outros em um todo (o prato de massa, por exemplo).
Esses tipos de hidrocarbonetos são encontrados naturalmente no gás natural e em campos de petróleo. Os mais leves apresentam características lubrificantes, enquanto os pesados se comportam como um asfalto indesejável; solúvel, entretanto, em parafinas. Eles servem muito bem como solventes, lubrificantes, combustíveis e asfalto.
Índice do artigo
- 1 Estrutura de alcanos lineares
- 1.1 Grupos
- 1.2 Comprimentos de suas correntes
- 1.3 Conformações
- 2 propriedades
- 2.1 Físico
- 2.2 Interações
- 2.3 Estabilidade
- 3 Nomenclatura
- 4 exemplos
- 5 referências
Estrutura de alcanos lineares
Grupos
Foi mencionado que a fórmula geral desses alcanos é CnH2n + 2. Esta fórmula é a mesma para todos os alcanos, sejam eles lineares ou ramificados. A diferença então no n- que precede a fórmula para alcano, cuja denotação significa "normal".
Veremos mais tarde que este n- é desnecessário para alcanos com um número de carbono igual ou inferior a quatro (n ≤ 4).
Uma linha ou cadeia não pode consistir em um único átomo de carbono, então metano (CH4, n = 1). Se n = 2, temos etano, CH3-CH3. Observe que este alcano consiste em dois grupos metil, CH3, ligados em conjunto.
Aumentando o número de carbonos, n = 3, dá o alcano propano, CH3-CHdois-CH3. Agora um novo grupo aparece, CHdois, chamado metileno. Não importa o quão grande seja o alcano linear, ele sempre terá apenas dois grupos: CH3 e CHdois.
Comprimentos de suas correntes
Quando n ou o número de carbonos no alcano linear aumenta, há uma constante em todas as estruturas resultantes: o número de grupos de metileno aumenta. Por exemplo, suponha que alcanos lineares com n = 4, 5 e 6:
CH3-CHdois-CHdois-CH3 (n-butano)
CH3-CHdois-CHdois-CHdois-CH3 (n-pentano)
CH3-CHdois-CHdois-CHdois-CHdois-CH3 (n-hexano)
As cadeias tornam-se mais longas porque adicionam grupos CH às suas estruturasdois. Assim, um alcano linear longo ou curto difere em quantos CHdois separa os dois grupos terminais CH3. Todos esses alcanos têm apenas dois desses CH3: no início e no final da string. Se eu tivesse mais, isso implicaria na presença de ramos.
Da mesma forma, pode ser observada a ausência total de grupos CH, presentes apenas nas ramificações ou quando há grupos substituintes ligados a um dos carbonos da cadeia.
A fórmula estrutural pode ser resumida da seguinte forma: CH3(CHdois)n-2CH3. Tente aplicá-lo e ilustrá-lo.
Conformações
Alguns alcanos lineares podem ser mais longos ou mais curtos do que outros. Sendo este o caso, n pode ter um valor de 2 a ∞; ou seja, uma cadeia composta de grupos CH infinitosdois e dois grupos CH3 terminais (teoricamente possíveis). No entanto, nem todas as strings são "acomodadas" da mesma maneira no espaço..
É aqui que surgem as conformações estruturais dos alcanos. O que eles devem? Para a rotabilidade das ligações C-H e sua flexibilidade. Quando esses elos giram ou giram em torno de um eixo internuclear, as correntes começam a se flexionar, dobrar ou enrolar, afastando-se de sua característica linear original..
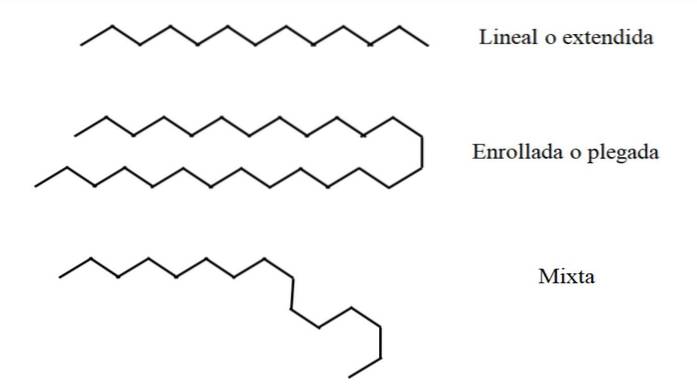
Linear
Na imagem superior, por exemplo, uma cadeia de treze carbonos é mostrada no topo que permanece linear ou estendida. Essa conformação é ideal, uma vez que se assume que o ambiente molecular afeta minimamente o arranjo espacial dos átomos na cadeia. Nada a perturba e ela não precisa se curvar.
Enrolado ou dobrado
No meio da imagem, a cadeia de 27 carbonos sofre uma perturbação externa. A estrutura, para ser mais "confortável", gira seus elos de maneira que se dobre sobre si mesma; como um espaguete comprido.
Estudos computacionais mostraram que o número máximo de carbonos que uma cadeia linear pode ter é n = 17. A partir de n = 18, é impossível que ela não comece a se dobrar ou se enrolar.
Misturado
Se a corrente for muito longa, pode haver regiões da corrente que permanecem lineares enquanto outras foram dobradas ou enroladas. De tudo, esta é talvez a conformação mais próxima da realidade.
Propriedades
Fisica
Sendo hidrocarbonetos, eles são essencialmente apolares e, portanto, hidrofóbicos. Isso significa que eles não podem se misturar com água. Eles não são muito densos porque suas correntes deixam muitos espaços vazios entre eles.
Da mesma forma, seus estados físicos variam de gasoso (para n < 5), líquidos (para n < 13) o sólidos (para n ≥ 14), y dependen de la longitud de la cadena.
Interações
As moléculas de alcanos lineares são apolares e, portanto, suas forças intermoleculares são do tipo de dispersão London. As cadeias (provavelmente adotando uma conformação mista), são então atraídas pela ação de suas massas moleculares e os dipolos induzidos instantâneos de seus átomos de hidrogênio e carbono..
É por esta razão que quando a corrente se torna mais longa e, portanto, mais pesada, seus pontos de ebulição e fusão aumentam da mesma forma..
Estabilidade
Quanto mais longa a corrente, mais instável ela é. Eles geralmente quebram seus elos para fazer correntes menores a partir de uma grande. Na verdade, esse processo é conhecido como rachaduras, altamente utilizado no refino de petróleo.
Nomenclatura
Para nomear alcanos lineares, basta adicionar o indicador n antes do nome. Se n = 3, como com o propano, é impossível para este alcano apresentar qualquer ramificação:
CH3-CHdois-CH3
O que não acontece depois de n = 4, ou seja, com n-butano e os outros alcanos:
CH3-CHdois-CHdois-CH3
OU
(CH3)doisCH-CH3
A segunda estrutura corresponde ao isobutano, que consiste em um isômero estrutural do butano. Para diferenciar um do outro, o indicador n entra em ação. Assim, o n-butano refere-se ao isômero linear apenas, sem ramificações.
Quanto maior o n, maior o número de isômeros estruturais e mais importante será usar n- para se referir ao isômero linear.
Por exemplo, octanagem, C8H18 (C8H8 × 2 + 2), tem até treze isômeros estruturais, uma vez que muitos ramos são possíveis. O isômero linear, no entanto, é denominado: n-octanagem, e sua estrutura é:
CH3-CHdois-CHdois-CHdois-CHdois-CHdois-CHdois-CH3
Exemplos
Eles são mencionados abaixo e para finalizar alguns alcanos lineares:
-Etano (CdoisH6): CH3CH3
-Propano (C3H8): CH3CHdoisCH3
-n-Heptano (C7H16): CH3(CHdois)5CH3.
- n-Dean (C10H22): CH3(CHdois)8CH3.
-n-Hexadecano (C16H3. 4): CH3(CHdois)14CH3.
-n-Nonadecano (C19H40): CH3(CHdois)17CH3.
-n-Eicosano (CvinteH42): CH3(CHdois)18CH3.
- n-Hectano (C100H202): CH3(CHdois)98CH3.
Referências
- Carey F. (2008). Quimica Organica. (Sexta edição). Mc Graw Hill.
- Morrison, R. T. e Boyd, R, N. (1987). Quimica Organica. (5ª Edição). Editorial Addison-Wesley Interamericana.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Química orgânica. Aminas. (10ª edição). Wiley plus.
- Jonathan M. Goodman. (1997). Qual é o alcano não ramificado mais longo com uma conformação global mínima linear? J. Chem. Inf. Comput. Sci. 1997, 37, 5, 876-878.
- Garcia Nissa. (2019). O que são alcanos? Estudar. Recuperado de: study.com
- Sr. Kevin A. Boudreaux. (2019). Alcanos. Recuperado de: angelo.edu
- Lista de alcenos de cadeia linear. [PDF]. Recuperado de: laney.edu
- Helmenstine, Anne Marie, Ph.D. (7 de setembro de 2018). Nomeie os primeiros 10 alcanos. Recuperado de: Thoughtco.com
- Ciência Quirky. (20 de março de 2013). Alcanos de cadeia linear: propriedades de previsão. Recuperado de: quirkyscience.com
- Wikipedia. (2019). Alcanos superiores. Recuperado de: en.wikipedia.org


Ainda sem comentários