
Anidridos ácidos, como são formados, aplicações e exemplos

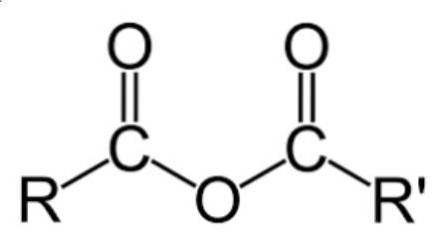
O anidridos de ácido são considerados de grande importância entre a grande variedade de compostos de origem orgânica existentes. Estas são apresentadas como moléculas que possuem dois grupos acila (substituintes orgânicos cuja fórmula é RCO-, onde R é uma cadeia de carbono) ligados ao mesmo átomo de oxigênio..
Além disso, há uma classe de anidridos de ácido comumente encontrada: anidridos carboxílicos, assim chamados porque o ácido inicial é um ácido carboxílico. Para nomear aqueles deste tipo cuja estrutura é simétrica, apenas uma substituição de termos deve ser feita.
O termo ácido na nomenclatura de seu ácido carboxílico original deve ser substituído pelo termo anidrido, que significa "sem água", sem alterar o restante do nome da molécula formada. Estes compostos também podem ser gerados a partir de um ou dois grupos acila de outros ácidos orgânicos, tais como ácido fosfônico ou ácido sulfônico..
Da mesma forma, os anidridos de ácido podem ser produzidos com base em um ácido inorgânico, como o ácido fosfórico. No entanto, suas propriedades físicas e químicas, suas aplicações e outras características dependem da síntese realizada e da estrutura do anidrido..
Índice do artigo
- 1 Como os anidridos de ácido são formados?
- 2 Fórmula geral
- 3 aplicativos
- 3.1 Uso industrial
- 4 Exemplos de anidridos de ácido
- 5 referências
Como os anidridos de ácido são formados?
Alguns anidridos de ácido se originam de várias maneiras, tanto no laboratório quanto na indústria. Na síntese industrial, um exemplo é o anidrido acético, que é produzido principalmente por meio do processo de carbonilação da molécula de acetato de metila..
Outro exemplo dessas sínteses é o do anidrido maleico, gerado pela oxidação da molécula de benzeno ou de butano..
Porém, na síntese de anidridos ácidos em laboratório, a ênfase é colocada na desidratação dos ácidos correspondentes, como a produção de anidrido etanóico, em que duas moléculas de ácido etanóico são desidratadas para dar origem ao referido composto..
A desidratação intramolecular também pode ocorrer; ou seja, dentro da mesma molécula um ácido com dois grupos carboxila (ou dicarboxílicos), mas se ocorrer o oposto e um anidrido ácido sofrer hidrólise, ocorre a regeneração dos ácidos que o originaram.
Os anidridos ácidos cujos substituintes de acila são iguais são chamados simétricos, enquanto que em anidridos mistos desse tipo essas moléculas de acila são diferentes.
No entanto, essas espécies também são geradas quando ocorre uma reação entre um halogeneto de acila (cuja fórmula geral é (RCOX)) com uma molécula de carboxilato (cuja fórmula geral é R'COO-)). [dois]
Fórmula geral
A fórmula geral para anidridos de ácido é (RC (O))doisOu, o que é melhor visto na imagem colocada no início deste artigo.
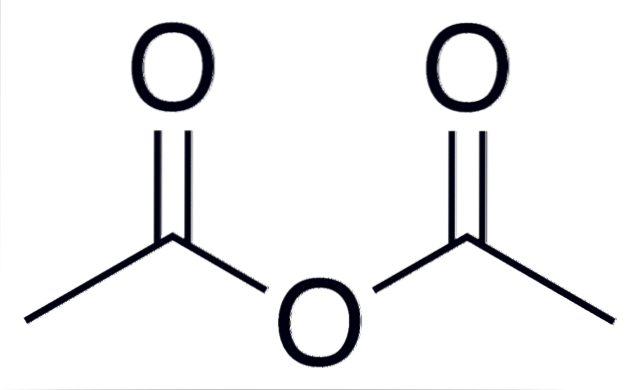
Por exemplo, para anidrido acético (de ácido acético), a fórmula geral é (CH3CO)doisOu, escrito da mesma forma para muitos outros anidridos de ácido semelhantes.
Como mencionado anteriormente, esses compostos têm quase o mesmo nome de seus ácidos precursores, e a única coisa que muda é o termo ácido para anidrido, já que as mesmas regras de numeração de átomos e substituintes devem ser seguidas para que sua nomenclatura seja correta..
Formulários
Os anidridos ácidos têm muitas funções ou aplicações dependendo do campo em estudo, pois, por apresentarem alta reatividade, podem ser precursores reativos ou fazer parte de muitas reações importantes..
Um exemplo disso é a indústria, onde o anidrido acético é produzido em grandes quantidades por possuir a estrutura mais simples que pode ser isolada. Este anidrido é usado como reagente em importantes sínteses orgânicas, como ésteres de acetato..
Uso industrial
Já o anidrido maleico apresenta estrutura cíclica, sendo utilizado na produção de revestimentos para uso industrial e como precursor de algumas resinas pelo processo de copolimerização com moléculas de estireno. Além disso, essa substância atua como um dienófilo quando a reação de Diels-Alder é realizada..
Da mesma forma, existem compostos que possuem duas moléculas de anidridos de ácido em sua estrutura, como o dianidrido etilenotetracarboxílico ou o dianidrido benzoquinonetetracarboxílico, que são utilizados na síntese de certos compostos como as poliimidas ou algumas poliamidas e poliésteres..
Além destes, existe um anidrido misto denominado 3'-fosfoadenosina-5'-fosfosulfato, proveniente dos ácidos fosfórico e sulfúrico, que é a coenzima mais comum nas reações biológicas de transferência de sulfato..
Exemplos de anidridos de ácido
Abaixo está uma lista com os nomes de alguns anidridos de ácido, para dar alguns exemplos desses compostos tão importantes na química orgânica que podem formar compostos de estrutura linear ou anéis com vários membros:
- Anidrido acético.
- Anidrido propanóico.
- Anidrido benzóico.
- Anidrido maleico.
- Anidrido succínico.
- Anidrido ftálico.
- Dianidrido naftaleno tetracarboxílico.
- Dianidrido etilenotetracarboxílico.
- Dianidrido benzoquinonetetracarboxílico.
Assim como esses anidridos são formados com o oxigênio, existem outros compostos onde um átomo de enxofre pode substituir o oxigênio tanto no grupo carbonila quanto no oxigênio central, tais como:
- Anidrido tioacético (CH3C (S)doisOU)
Há até o caso de duas moléculas de acila que formam ligações com o mesmo átomo de enxofre; esses compostos são chamados tioanidridos, a saber:
- Tioanidrido acético ((CH3CO))doisS)
Referências
- Wikipedia. (2017). Wikipedia. Recuperado de en.wikipedia.org
- Johnson, A. W. (1999). Convite para Química Orgânica. Recuperado de books.google.co.ve.
- Acton, Q. A. (2011). Hidrolases de anidrido ácido: avanços em pesquisa e aplicação. Recuperado de books.google.co.ve
- Bruckner, R. e Harmata, M. (2010). Mecanismos orgânicos: reações, estereoquímica e síntese. Recuperado de books.google.co.ve
- Kim, J. H., Gibb, H. J. e Iannucci, A. (2009). Anidridos de ácido cíclico: Aspectos da saúde humana. Recuperado de books.google.co.ve


Ainda sem comentários