
Estrutura, propriedades, usos do borohidreto de sódio (NaBH4)

O Boro-hidreto de sódio é um sólido inorgânico cuja fórmula química é NaBH4. Pode ser considerado representativo dos borohidretos alcalinos e é o mais comum deles. É um sólido cristalino branco.
Quando em contato com a água, NaBH4 pode gerar calor e hidrogênio Hdois que é combustível, por isso deve ser manuseado com cuidado. Devido à facilidade com que pode gerar íons hidreto H-, o borohidreto de sódio é um composto moderadamente redutor, por isso é amplamente utilizado em reações químicas para esta finalidade.

Sua propriedade redutora também é utilizada na indústria de papel, pois melhora as características de alvura e estabilidade da celulose e do papel por atuar contra a oxidação da celulose, principal componente do papel..
Como pode facilmente formar hidrogênio na presença de água, a possibilidade de usá-lo como fonte reversível de hidrogênio em células a combustível também foi investigada..
Tem outros usos todos baseados em sua propriedade redutora, como na indústria farmacêutica.
Índice do artigo
- 1 Estrutura
- 2 Nomenclatura
- 3 propriedades físicas
- 3.1 Estado físico
- 3.2 Peso molecular
- 3.3 Temperatura de autoignição
- 3.4 Temperatura de decomposição
- 3,5 Densidade
- 3.6 Solubilidade
- 4 propriedades químicas
- 5 riscos
- 6 Obtendo
- 7 usos
- 7.1 Em reações químicas de redução
- 7.2 Na produção de H2 em células de combustível
- 7.3 Na indústria de celulose e papel
- 7.4 Em vários usos
- 8 referências
Estrutura
O borohidreto de sódio é um composto iônico. É formado pelo ânion borohidreto [BH4]- ligado ao cátion sódio Na+.
O ânion [BH4]- é tetraédrico.
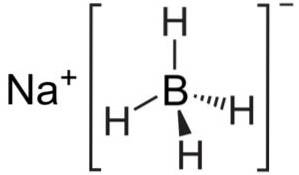
Sua estrutura de Lewis é a seguinte:
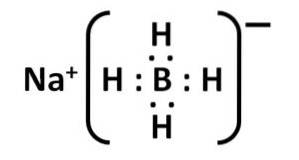
Nomenclatura
-Boro-hidreto de sódio
-Tetrahidroborato de sódio
-Tetrahidruroborato de sódio
Propriedades físicas
Estado físico
Sólido branco cristalino.
Peso molecular
37,84 g / mol
Temperatura de autoignição
∼ 220 ºC
temperatura de decomposição
> 250 ºC
Densidade
1.074 g / cm3 a 20 ºC
Solubilidade
O NaBH4 é bastante solúvel em água (55 g / 100mL a 25 ºC), onde é parcialmente hidrolisado. É solúvel em tetrahidrofurano (THF) e é insolúvel em éter dietílico.
Propriedades quimicas
O borohidreto de sódio se dissolve na água, onde sofre decomposição inicial ou hidrólise que torna a solução básica, evitando hidrólise posterior..
[BH4]- + HdoisO → B (OH)3 + Hdois↑ + OH-
Isso é explicado porque o [BH4]- interage com o H+ da água, onde o H+ leva um ânion hidreto H- para formar Hdois. Pode-se dizer que o BH3 competir com o H+ pelo íon hidreto H-.
Em um meio ácido a hidrólise é completa devido à abundância de íons H+.
O NaBH4 é estável ao ar seco. Não é volátil.
Devido ao seu conteúdo de íons hidreto, o borohidreto de sódio é um composto redutor. Permite reduzir o grupo carbonila C = O a C-OH, ou seja, compostos carbonila a álcoois.
O NaBH4 Por si só não reduz as ligações duplas C = C, nem mesmo aquelas conjugadas com grupos carbonil -C = C-C (= O)-.
No entanto, quando em contato com ácidos protônicos (como HCl) ou ácidos de Lewis (como BCl3 ou AlCl3) diborano B é formadodoisH6. E se esta reação for realizada na presença de compostos orgânicos com ligações duplas C = C, o diborano BdoisH6 realiza a hidroboração destes.
Na presença de catalisadores apropriados e condições específicas, o boro-hidreto de sódio pode reduzir vários tipos de grupos funcionais.
Riscos
O calor da reação de hidrólise na água é suficiente para inflamar o hidrogênio que se forma nela. Portanto, é importante ter cuidado ao lidar com isso.
O NaBH4 é facilmente inflamado e queima facilmente.
Obtendo
A reação típica de preparação de NaBH4 é através de hidreto de sódio NaH e B (OCH3)3 a uma temperatura de cerca de 250 ºC:
4 NaH + B (OCH3)3 → NaBH4 + 3 NaOCH3
Formulários
Em reações químicas de redução
Porque é uma fonte de íons H-, o NaBH4 É um composto redutor e é usado para preparar outros compostos químicos. Para isso é utilizado em solventes polares apróticos, ou seja, sem prótons H+, tais como dimetilsulfóxido, hexametilfosforamida e dimetilformamida.
É usado como agente redutor em reações químicas orgânicas e inorgânicas..
Permite reduzir aldeídos a álcoois primários e cetonas a álcoois secundários.
Também reduz haletos de alquila a hidrocarbonetos, como iododecano a decano, ácido bromoundecanóico a ácido undecanóico e clorododecano a dodecano..
Se atuar sozinho, ao realizar a redução não afeta outros grupos funcionais como éster, ácido carboxílico, nitrila e sulfona.
Sua propriedade de não reduzir as ligações duplas C = C, nem mesmo aquelas conjugadas com grupos carbonila -C = C-C (= O) -, possibilita a preparação de álcoois insaturados -C = C-CHdois-Oh.
Para reduzir os compostos aromáticos nitrados às suas anilinas correspondentes, é necessária a presença de catalisadores como o cobalto ou o cloreto de estanho. Reduz dissulfetos a tióis.
Na presença de condições e catalisadores adequados, permite reduzir os ácidos carboxílicos, ésteres, amidas, nitrilos, iminas, epóxidos e até mesmo ligações duplas e triplas.
Na produção de Hdois em células de combustível
O NaBH4 pode ser convertido em uma célula de combustível.
O NaBH4 na presença de uma solução alcalina de KOH ou NaOH ele hidrolisa e produz hidrogênio Hdois que pode ser usado como combustível em uma célula de combustível de eletrólito de polímero.
Também foi investigado como um material de armazenamento para Hdois reversivelmente.
Nanopartículas de NaBH são sintetizadas4 e estabilizado com um surfactante. Após o tratamento com NiCldois uma camada protetora ou revestimento é formado que regula a liberação de Hdois completamente reversível.
Este novo material nanométrico permitiria o uso de Hdois como um combustível limpo e renovável.

Na indústria de celulose e papel
O borohidreto de sódio é usado para melhorar o brilho e outras propriedades físicas da celulose e do papel..
A degradação da matriz celulósica do papel ocorre por meio de processos complexos que envolvem oxidação. Os grupos hidroxila são oxidados a carbonila e carboxila, o que leva à descoloração do papel e diminuição de suas propriedades físicas..
Ao tratar polpa ou papel com NaBH4, Isso reduz aldeídos e cetonas a grupos -OH sem afetar os grupos carboxílicos ácidos, melhorando a estabilidade e o brilho em valores superiores aos iniciais..

Em vários usos
El borohidruro de sodio se emplea para tratar aguas de desecho, como agente mejorador del sabor en la industria de alimentos y bebidas, como agente de recubrimiento y para el tratamiento de superficies, en la producción de tabaco, en la industria farmacéutica, de textiles y de couro.
Referências
- Christian, M.L. e Aguey-Zinsou, K.-F. (2012). Estratégia Core-Shell que leva a alta capacidade de armazenamento de hidrogênio reversível para NaBH4. ACS Nano 2012, 6, 9, 7739-7751. Recuperado de pubs.acs.org.
- Nora de Souza, M.V. e Alves V., T.R. (2006). Metodologias recentes mediadas por borohidreto de sódio na redução de diferentes classes de compostos. App. Organometal. Chem. 2006; 20: 798-810. Recuperado de onlinelibrary.wiley.com.
- Imamoto, T. (1991). Redução. Boro-hidreto de sódio. In Comprehensive Organic Synthesis. Recuperado de sciencedirect.com.
- Tang, L.C. (1986) Stabilization of Paper through Sodium Borohydride Treatment. Em Têxteis Históricos e Materiais de Papel. Capítulo 24. Páginas 427-441. Advances in Chemistry, Volume 212. Recuperado de pubs.acs.org.
- Cotton, F. Albert e Wilkinson, Geoffrey. (1980). Química Inorgânica Avançada. Quarta edição. John Wiley & Sons.
- Morrison, Robert Thornton; e Boyd, Robert Neilson. 1992. Organic Chemistry. Prentice-Hall. ISBN 81-203-0765-8.
- NÓS. Biblioteca Nacional de Medicina. (2019). Boro-hidreto de sódio. Recuperado de: pubchem.ncbi.nlm.nih.gov.



Ainda sem comentários