
Características e exemplos do carbono anomérico
O carbono anomérico é um estereocentro presente nas estruturas cíclicas dos carboidratos (mono ou polissacarídeos). Por ser um estereocentro, mais precisamente um epímero, dele derivam dois diastereoisômeros, designados pelas letras α e β; estes são os anômeros e fazem parte da extensa nomenclatura do mundo dos açúcares.
Cada anômero, α ou β, difere na posição do grupo OH do carbono anomérico em relação ao anel; mas em ambos o carbono anomérico é o mesmo e está localizado no mesmo lugar na molécula. Anômeros são hemiacetais cíclicos, produto de uma reação intramolecular na cadeia aberta de açúcares; se aldoses (aldeídos) ou cetoses (cetonas).
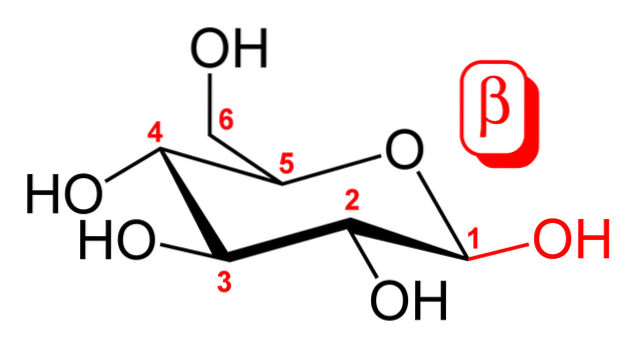
A imagem superior mostra a conformação da cadeira para β-D-glucopiranose. Como pode ser visto, ele consiste em um anel de seis membros, incluindo um átomo de oxigênio entre os carbonos 5 e 1; o último, ou melhor, o primeiro, é o carbono anomérico, que forma duas ligações simples com dois átomos de oxigênio.
Se você olhar de perto, o grupo OH ligado ao carbono 1 está orientado acima do anel hexagonal, assim como o grupo CHdoisOH (carbono 6). Este é o anômero β. Já o anômero α diferiria apenas neste grupo OH, que estaria localizado abaixo do anel, como se fosse um diastereoisômero trans..
Índice do artigo
- 1 hemicetais
- 1.1 Hemiacetal cíclico
- 2 Características do carbono anomérico e como reconhecê-lo
- 3 exemplos
- 3.1 Exemplo 1
- 3.2 Exemplo 2
- 3.3 Exemplo 3
- 4 referências
Hemicetais
É necessário aprofundar um pouco mais no conceito de hemiacetais para melhor compreender e distinguir o carbono anomérico. Os hemicetais são o produto de uma reação química entre um álcool e um aldeído (aldoses) ou uma cetona (cetoses).
Esta reação pode ser representada pela seguinte equação química geral:
ROH + R'CHO => ROCH (OH) R '
Como pode ser visto, um álcool reage com um aldeído para formar o hemiacetal. O que aconteceria se R e R 'pertencessem à mesma cadeia? Nesse caso, você teria um hemiacetal cíclico, e a única maneira possível de se formar é que ambos os grupos funcionais, -OH e -CHO, estejam presentes na estrutura molecular..
Além disso, a estrutura deve ser constituída por uma cadeia flexível, e com ligações capazes de facilitar o ataque nucleofílico do OH ao carbono carbonílico do grupo CHO. Quando isso acontece, a estrutura se fecha em um anel de cinco ou seis membros..
Hemiacetal cíclico
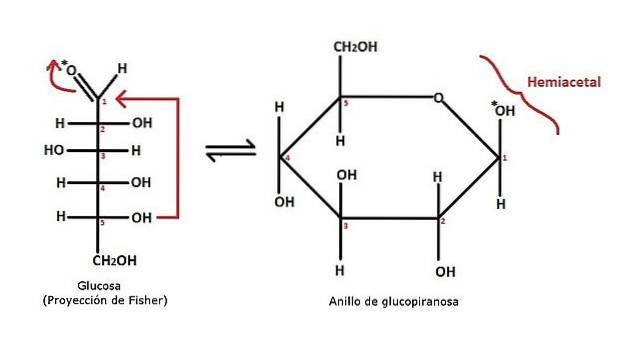
Um exemplo da formação de um hemiacetal cíclico para monossacarídeo de glicose é mostrado na imagem acima. Pode ser visto como consistindo de uma aldose, com um grupo aldeído CHO (carbono 1). Este é atacado pelo grupo OH do carbono 5, conforme indicado pela seta vermelha.
A estrutura passa de uma cadeia aberta (glicose), a um anel pirano (glicopiranose). A princípio, pode não haver relação entre essa reação e a que acabamos de explicar para o hemiacetal; mas se você olhar cuidadosamente para o anel, especificamente na seção C5-O-C1(OH) -Cdois, será apreciado que isto corresponde ao esqueleto esperado para um hemiacetal.
Os carbonos 5 e 2 passam a representar R e R 'da equação geral, respectivamente. Como fazem parte da mesma estrutura, é então um hemiacetal cíclico (e o anel é suficiente para ficar evidente).
Características do carbono anomérico e como reconhecê-lo
Onde está o carbono anomérico? Na glicose, este é o grupo CHO, que pode sofrer ataque nucleofílico por OH de baixo ou de cima. Dependendo da orientação do ataque, dois anômeros diferentes são formados: α e β, como já mencionado..
Portanto, uma primeira característica que este carbono possui é que na cadeia aberta do açúcar é aquele que sofre o ataque nucleofílico; ou seja, é o grupo CHO, para as aldoses, ou o grupo RdoisC = O, para cetoses. No entanto, uma vez que o hemiacetal ou anel cíclico é formado, esse carbono pode parecer ter desaparecido..
É aqui que existem outras características mais específicas para localizá-lo em qualquer anel pirano ou furanose de todos os carboidratos:
-O carbono anomérico está sempre à direita ou esquerda do átomo de oxigênio que compõe o anel.
-Mais importante ainda, está ligado não só a este átomo de oxigênio, mas também ao grupo OH, vindo de CHO ou RdoisC = O.
-É assimétrico, ou seja, possui quatro substituintes diferentes.
Com essas quatro características, é fácil reconhecer o carbono anomérico observando qualquer "estrutura doce".
Exemplos
Exemplo 1
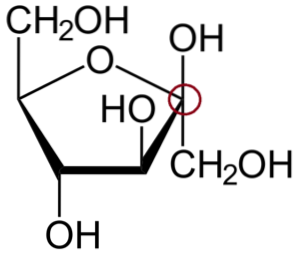
Acima está β-D-frutofuranose, um hemiacetal cíclico com um anel de cinco membros..
Para identificar o carbono anomérico, você deve primeiro olhar para os carbonos nos lados esquerdo e direito do átomo de oxigênio que compõe o anel. Então, aquele que está ligado ao grupo OH é o carbono anomérico; que, neste caso, já está circulado em vermelho.
Este é o anômero β porque o OH do carbono anomérico está acima do anel, assim como o grupo CHdoisOh.
Exemplo 2
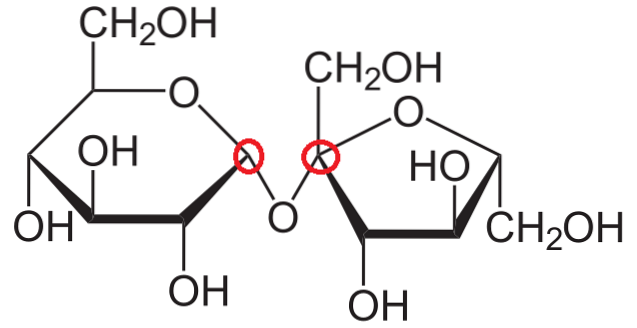
Agora, tentamos explicar quais são os carbonos anoméricos na estrutura da sacarose. Como pode ser visto, ele consiste em dois monossacarídeos covalentemente ligados por uma ligação glicosídica, -O-.
O anel da direita é exatamente o mesmo que acabamos de mencionar: β-D-frutofuranose, só que “virado” para a esquerda. O carbono anomérico permanece o mesmo do caso anterior e atende a todas as características que dele seriam esperadas.
Por outro lado, o anel à esquerda é α-D-glucopiranose.
Repetindo o mesmo procedimento de reconhecimento de carbono anomérico, olhando para os dois carbonos do lado esquerdo e direito do átomo de oxigênio, verifica-se que o carbono direito é aquele que está ligado ao grupo OH; que participa da ligação glicosídica.
Portanto, ambos os carbonos anoméricos são conectados pela ligação -O- e, portanto, eles estão incluídos em círculos vermelhos..
Exemplo 3
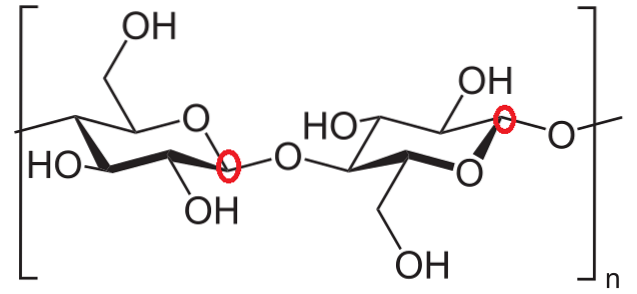
Por fim, propõe-se identificar os carbonos anoméricos de duas unidades de glicose na celulose. Novamente, os carbonos ao redor do oxigênio dentro do anel são observados, e é descoberto que no anel de glicose à esquerda o carbono anomérico participa da ligação glicosídica (dentro do círculo vermelho).
No anel de glicose à direita, entretanto, o carbono anomérico está à direita do oxigênio e é facilmente identificado porque está ligado ao oxigênio da ligação glicosídica. Assim, ambos os carbonos anoméricos são totalmente identificados.
Referências
- Morrison, R. T. e Boyd, R, N. (1987). Quimica Organica. 5ta Edição. Editorial Addison-Wesley Interamericana.
- Carey F. (2008). Quimica Organica. (Sexta edição). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Química orgânica. Aminas. (10º edição.). Wiley plus.
- Rendina G. (1974). Técnicas de bioquímica aplicada. Interamericana, México.
- Chang S. (s.f.). Um guia para o carbono anomérico: o que é um carbono anomérico? [PDF]. Recuperado de: chem.ucla.edu
- Gunawardena G. (13 de março de 2018). Carvão anomérico. Chemistry LibreTexts. Recuperado de: chem.libretexts.org
- Foist L. (2019). Carbono anomérico: definição e visão geral. Estudar. Recuperado de: study.com



Ainda sem comentários