
Características da glutationa, estrutura, funções, biossíntese
O glutationa (GSH) é uma pequena molécula tripeptídica (com apenas três resíduos de aminoácidos) não proteica que participa de muitos fenômenos biológicos, como mecânica enzimática, biossíntese de macromoléculas, metabolismo intermediário, toxicidade do oxigênio, transporte intracelular, etc..
Este pequeno peptídeo, presente em animais, plantas e algumas bactérias, é considerado um "amortecedor" oxido-redutor, por ser um dos principais compostos de baixo peso molecular que contém enxofre e carece da toxicidade associada aos resíduos de cisteína.
Algumas doenças em humanos têm sido associadas à deficiência de enzimas específicas do metabolismo da glutationa, e isso se deve às suas múltiplas funções na manutenção da homeostase corporal.
A desnutrição, o estresse oxidativo e outras patologias sofridas pelos humanos podem ser evidenciadas como uma diminuição drástica da glutationa, razão pela qual às vezes é um bom indicador do estado de saúde dos sistemas do corpo.
Para as plantas, da mesma forma, a glutationa é um fator essencial para o seu crescimento e desenvolvimento, pois também desempenha funções em múltiplas vias biossintéticas e é essencial para a desintoxicação celular e homeostase interna, onde atua como um poderoso antioxidante..
Índice do artigo
- 1 recursos
- 2 Estrutura
- 3 funções
- 3.1 Coenzima
- 3.2 Armazenamento de cisteína
- 3.3 Enrolamento de proteínas
- 3.4 Função em eritrócitos
- 3,5 Metabolismo xenobiótico
- 3.6 Estado oxidativo das células
- 4 Biossíntese
- 4.1 Glutationa reduzida (GSH)
- 4.2 Glutationa oxidada (GSSG)
- 5 benefícios de sua ingestão
- 5.1 Câncer
- 5,2 HIV
- 5.3 Atividade muscular
- 5.4 Patologias hepáticas
- 5,5 antioxidante
- 5.6 "Absorção"
- 6 efeitos colaterais
- 7 referências
Caracteristicas
Os primeiros estudos realizados em relação à localização subcelular da glutationa mostraram que ela está presente na mitocôndria. Posteriormente, também foi observado na região correspondente à matriz nuclear e nos peroxissomos..
Atualmente, sabe-se que o compartimento onde sua concentração é mais abundante é no citosol, uma vez que ali é produzido ativamente e transportado para outros compartimentos celulares, como a mitocôndria..
Em células de mamíferos, a concentração de glutationa está na faixa dos milimoles, enquanto no plasma sanguíneo sua forma reduzida (GSH) é encontrada em concentrações micromolares..
Essa concentração intracelular se assemelha muito à concentração de glicose, potássio e colesterol, elementos essenciais para a estrutura, função e metabolismo celulares..
Alguns organismos têm moléculas de glutationa análogas ou variantes. Os parasitas protozoários que afetam os mamíferos têm uma forma conhecida como "tripanotion" e, em algumas bactérias, esse composto é substituído por outras moléculas de enxofre, como o tiossulfato e a glutamilcisteína..
Certas espécies de plantas possuem, além da glutationa, moléculas homólogas que possuem resíduos diferentes da glicina na extremidade C-terminal (homoglutationa) e que são caracterizadas por terem funções semelhantes às do tripeptídeo em questão..
Apesar da existência de outros compostos semelhantes à glutationa em diferentes organismos, este é um dos "tióis" encontrados em maior concentração intracelular..
A alta proporção que normalmente existe entre a forma reduzida (GSH) e a forma oxidada (GSSG) da glutationa é outra característica distintiva desta molécula..
Estrutura
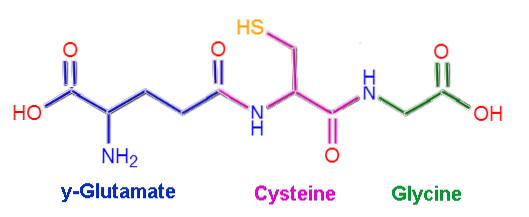
A glutationa ou L-γ-glutamil-L-cisteinil-glicina, como o próprio nome indica, é composta por três resíduos de aminoácidos: L-glutamato, L-cisteína e glicina. Os resíduos de cisteína e glicina estão ligados entre si por meio de ligações peptídicas comuns, ou seja, entre o grupo α-carboxila de um aminoácido e o grupo α-amino do outro..
No entanto, a ligação que ocorre entre o glutamato e a cisteína não é típica das proteínas, uma vez que ocorre entre a porção γ-carboxila do grupo R do glutamato e o grupo α-amino da cisteína. É chamada de ligação γ.
Essa pequena molécula tem massa molar de pouco mais de 300 g / mol e a presença da ligação γ parece ser crucial para a imunidade desse peptídeo contra a ação de muitas enzimas aminopeptidases..
Características
Como mencionado, a glutationa é uma proteína que participa de vários processos celulares em animais, plantas e certos procariontes. Nesse sentido, sua participação geral em:
-Os processos de síntese e degradação de proteínas
-A formação de precursores de ribonucleotídeos de DNA
-Regulação da atividade de algumas enzimas
-Proteção de células na presença de espécies reativas de oxigênio (ROS) e outros radicais livres
-Transdução de sinal
-Expressão genética e em
-Apoptose ou morte celular programada
Coenzima
A glutationa também foi determinada para funcionar como uma coenzima em muitas reações enzimáticas, e essa parte de sua importância está relacionada à sua capacidade de transportar aminoácidos na forma de γ-glutamil aminoácidos intracelularmente..
A glutationa que pode deixar a célula (o que faz em sua forma reduzida) é capaz de participar de reações de redução de oxidação na vizinhança da membrana plasmática e no ambiente celular circundante, o que protege as células de danos contra diferentes classes de agentes oxidantes.
Armazenamento de cisteína
Este tripéptido também funciona como fonte de armazenamento de cisteína e contribui para a manutenção do estado reduzido dos grupos sulfidrilo das proteínas no interior da célula e do estado ferroso do grupo heme das proteínas que contêm o referido cofactor..
Dobramento de proteínas
Quando participa do enovelamento de proteínas, parece ter uma função importante como agente redutor de pontes dissulfeto que foram formadas inadequadamente em estruturas de proteínas, o que geralmente é devido à exposição a agentes oxidantes como oxigênio, peróxido de hidrogênio, peroxinitrito e alguns superóxidos.
Função eritrocitária
Nos eritrócitos, a glutationa reduzida (GSH) produzida pela enzima glutationa redutase, que utiliza o NADPH produzido pela via da pentose fosfato, contribui para a remoção do peróxido de hidrogênio por meio da reação catalisada por outra enzima: a glutationa peroxidase, que produz água e glutationa oxidada (GSSG).
A quebra do peróxido de hidrogênio e, portanto, a prevenção de seu acúmulo nos eritrócitos, prolonga o tempo de vida dessas células, pois evita o dano oxidativo que pode ocorrer na membrana celular e que pode culminar em hemólise..
Metabolismo xenobiótico
A glutationa também desempenha um papel importante no metabolismo dos xenobióticos, graças à ação das enzimas glutationa S-transferase que geram conjugados de glutationa que podem ser metabolizados intracelularmente..
É prudente lembrar que o termo "xenobiótico" é usado para se referir a drogas, poluentes ambientais e carcinógenos químicos aos quais um organismo está exposto..
Estado oxidativo das células
Como a glutationa existe em duas formas, uma reduzida e outra oxidada, a relação entre as duas moléculas determina o estado redox das células. Se a relação GSH / GSSG for maior que 100, as células são consideradas saudáveis, mas se estiver próximo a 1 ou 10, pode ser um indicador de que as células estão em estado de estresse oxidativo.
Biossíntese
O tripeptídeo glutationa é sintetizado no interior das células, tanto em plantas quanto em animais, pela ação de duas enzimas: (1) γ-glutamilcisteína sintetase e (2) glutationa sintetase (GSH sintetase), enquanto sua degradação ou "decomposição" depende de a ação da enzima γ-glutamil transpeptidase.
Em organismos vegetais, cada uma das enzimas é codificada por um único gene e defeitos em qualquer uma das proteínas ou seus genes codificadores podem causar letalidade em embriões.
Em humanos, como em outros mamíferos, o principal local de síntese e exportação de glutationa é o fígado, especificamente nas células do fígado (hepatócitos) que circundam os dutos venosos que transportam sangue e outras substâncias de e para o órgão em questão.
Síntese de novo glutationa, sua regeneração ou reciclagem, requer energia do ATP para ocorrer.
Glutationa reduzida (GSH)
A glutationa reduzida é derivada dos aminoácidos glicina, glutamato e cisteína, como já mencionado, e sua síntese começa com a ativação (usando ATP) do grupo γ-carboxila do glutamato (do grupo R) para formar um fosfato de acila intermediário, que é atacado pelo grupo α-amino da cisteína.
Esta primeira reação de condensação de dois aminoácidos é catalisada pela γ-glutamilcisteína sintetase e é geralmente afetada pela disponibilidade intracelular dos aminoácidos glutamato e cisteína..
O dipeptídeo assim formado é posteriormente condensado com uma molécula de glicina graças à ação da GSH sintetase. Durante essa reação, também ocorre uma ativação com ATP do grupo α-carboxila da cisteína para formar um fosfato de acila e, assim, favorecer a reação com o resíduo de glicina..
Glutationa oxidada (GSSG)
Quando a glutationa reduzida participa das reações de redução de oxidação, a forma oxidada é, na verdade, composta de duas moléculas de glutationa ligadas entre si por meio de pontes dissulfeto; é por esta razão que a forma oxidada é abreviada com as iniciais "GSSG".
A formação da espécie oxidada de glutationa depende de uma enzima conhecida como glutationa peroxidase ou GSH peroxidase, que é uma peroxidase que contém uma selenocisteína (um resíduo de cisteína que em vez de ter um átomo de enxofre tem um átomo de selênio) no lugar . ativo.
A interconversão entre as formas oxidada e reduzida ocorre graças à participação de uma GSSG redutase ou glutationa redutase, que utiliza NAPDH para catalisar a redução de GSSG na presença de oxigênio, com a formação concomitante de peróxido de hidrogênio..
Benefícios de sua ingestão
A glutationa pode ser administrada por via oral, tópica, intravenosa, intranasal ou nebulizada, a fim de aumentar sua concentração sistêmica em pacientes que sofrem de estresse oxidativo, por exemplo.
Câncer
Pesquisas sobre a administração oral de glutationa sugerem que sua ingestão pode reduzir os riscos de câncer oral e que, quando administrada em conjunto com quimioterápicos oxidativos, reduz os efeitos negativos da terapia em pacientes com câncer..
HIV
Geralmente, os pacientes infectados com o vírus da imunodeficiência adquirida (HIV) têm deficiências de glutationa intracelular tanto nos glóbulos vermelhos quanto nas células T e monócitos, o que determina seu funcionamento correto.
Em um estudo de Morris et al., Foi demonstrado que o fornecimento de glutationa a macrófagos de pacientes HIV-positivos melhorou consideravelmente a função dessas células, especialmente contra infecções por patógenos oportunistas, como M. tuberculosis.
Atividade muscular
Outros estudos referem-se à melhora da atividade contrátil muscular, defesa antioxidativa e dano oxidativo causado em resposta a lesões de isquemia / reperfusão após administração oral de GSH durante o treinamento físico resistido..
Patologias hepáticas
Considera-se, por sua vez, que sua ingestão ou administração intravenosa tem funções na prevenção do progresso de alguns tipos de câncer e na redução do dano celular que ocorre em decorrência de certas patologias hepáticas..
Antioxidante
Embora nem todos os estudos relatados tenham sido realizados em pacientes humanos, mas geralmente sejam testes em modelos animais (geralmente murinos), os resultados obtidos em alguns ensaios clínicos confirmam a eficácia da glutationa exógena como antioxidante..
Por este motivo, é utilizado para o tratamento de cataratas e glaucoma, como um produto "anti-envelhecimento", para o tratamento de hepatites, numerosas doenças cardíacas, perda de memória e para fortalecer o sistema imunológico, e para a depuração após metais pesados e envenenamento por drogas.
"Absorção"
A glutationa administrada exogenamente não pode entrar nas células, a menos que seja hidrolisada em seus aminoácidos constituintes. Portanto, o efeito direto da administração (oral ou intravenosa) deste composto é o aumento da concentração intracelular de GSH graças à contribuição dos aminoácidos necessários à sua síntese, que podem ser efetivamente transportados para o citosol..
Efeitos secundários
Embora a ingestão de glutationa seja considerada "segura" ou inofensiva, não foram realizados estudos suficientes sobre seus efeitos colaterais..
Porém, dos poucos estudos relatados sabe-se que pode ter efeitos negativos decorrentes da interação com outras drogas e que podem ser prejudiciais à saúde em diversos contextos fisiológicos..
Se tomadas em longo prazo, parece que atuam diminuindo excessivamente os níveis de zinco e, além disso, se inaladas, podem produzir crises graves de asma em pacientes asmáticos..
Referências
- Allen, J., & Bradley, R. (2011). Efeitos da suplementação de glutationa oral em biomarcadores de estresse oxidativo sistêmico em voluntários humanos. The Journal of Alternative and Complementary Medicine, 17(9), 827-833.
- Conklin, K. A. (2009). Antioxidantes dietéticos durante a quimioterapia do câncer: impacto na eficácia quimioterápica e desenvolvimento de efeitos colaterais. Nutrição e Câncer, 37(1), 1-18.
- Meister, A. (1988). Metabolismo da glutationa e sua modificação seletiva. The Journal of Biological Chemistry, 263(33), 17205-17208.
- Meister, A., & Anderson, M. E. (1983). Glutationa. Ann. Rev Biochem., 52, 711-760.
- Morris, D., Guerra, C., Khurasany, M., Guilford, F., & Saviola, B. (2013). A suplementação de glutationa melhora as funções dos macrófagos no HIV. Journal of Interferon & Cytokine Research, onze.
- Murray, R., Bender, D., Botham, K., Kennelly, P., Rodwell, V., & Weil, P. (2009). Bioquímica Ilustrada de Harper (28ª ed.). McGraw-Hill Medical.
- Nelson, D. L., & Cox, M. M. (2009). Princípios de Bioquímica de Lehninger. Edições Omega (5ª ed.). https://doi.org/10.1007/s13398-014-0173-7.2
- Noctor, G., Mhamdi, A., Chaouch, S., Han, Y. I., Neukermans, J., Marquez-garcia, B.,… Foyer, C. H. (2012). Glutationa nas plantas: uma visão geral integrada. Planta, célula e meio ambiente, 35, 454-484.
- Pizzorno, J. (2014). Glutationa! Medicina Investigativa, 13(1), 8-12.
- Qanungo, S., Starke, D. W., Pai, H. V, Mieyal, J. J., & Nieminen, A. (2007). A suplementação de glutationa potencializa a apoptose hipóxica por S-glutationilação de p65-NFkB. The Journal of Biological Chemistry, 282(25), 18427-18436.
- Ramires, P. R., & Ji, L. L. (2001). A suplementação e o treinamento com glutationa aumentam a resistência do miocárdio à isquemia-reperfusão in vivo. Ann. J. Physiol. Heart Circ. Physiol., 281, 679-688.
- Sies, H. (2000). Glutationa e seu papel nas funções celulares. Biologia e Medicina Radicais Livres R, 27(99), 916-921.
- Wu, G., Fang, Y., Yang, S., Lupton, J. R., & Turner, N. D. (2004). Metabolismo da glutationa e suas implicações para a saúde. Sociedade Americana de Ciências Nutricionais, 489-492.


Ainda sem comentários