
Racional da reação de xantoproteína, procedimento, uso

O reação de xantoproteína é um procedimento químico usado para determinar a presença ou ausência de aminoácidos aromáticos, como tirosina e triptofano, que podem estar na forma livre ou constituindo proteínas, peptídeos ou polipeptídeos solúveis.
Também tem sido usado para detectar substâncias tóxicas no sangue que contêm um grupo benzeno em sua estrutura. Este teste também é conhecido como reação da xantoproteína Becher..
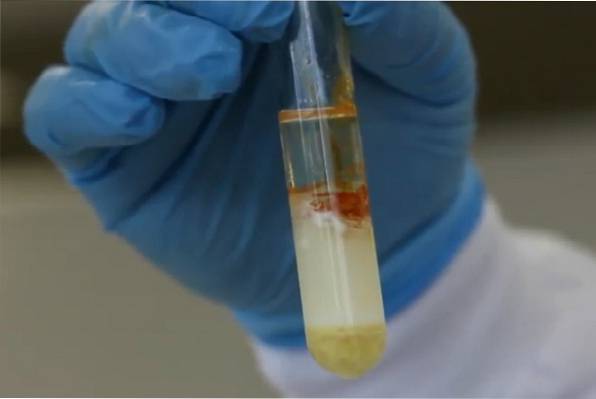
A reação da xantoproteína usa ácido nítrico concentrado, calor e um álcali neutralizante. Se a solução passar de amarelo para laranja quando a reação for neutralizada, o teste é considerado positivo. A coloração observada deve-se à formação de compostos nitrogenados derivados da nitrificação dos grupos benzênicos..
Se a quantidade de proteína total precisa ser quantificada, é necessário usar outros métodos de determinação de proteínas, como o Biureto..
A reação das xantoproteínas é utilizada principalmente quando estão sendo analisadas substâncias cuja composição química não é conhecida. Essa reação geralmente faz parte de um conjunto de testes que ajudarão a determinar a composição química de uma determinada substância ou extrato. É por isso que é amplamente utilizado por pesquisadores.
Por outro lado, a reação de xantoproteína de Becher é utilizada para detectar substâncias fenólicas e indol no sangue, permitindo predizer o aparecimento de nefropatia, antes que outros parâmetros posteriores sejam aumentados..
Índice do artigo
- 1 justificativa
- 2 Procedimento
- 2.1 - Reação de xantoproteína para detecção de aminoácidos com grupos aromáticos
- 2.2 - Reação de xantoproteína para detectar substâncias fenólicas e indol no sangue
- 3 Use
- 4 precauções
- 5 referências
Base
A reação detecta basicamente a presença do grupo benzeno, tanto em aminoácidos, como em proteínas e peptídeos. O ácido nítrico atua no anel benzênico dos aminoácidos que o possuem, formando compostos nitro fenólicos.
A reação precisa de calor para ser realizada, geralmente forma-se um precipitado que turva o meio, tornando-o leitoso. O precipitado pode ser branco ou amarelo. Finalmente, requer uma etapa de alcalinização que acentua a cor. Para isso, utiliza-se uma base como hidróxido de sódio a 40% ou amônia..
A reação será interpretada como positiva se uma forte coloração amarela for observada durante o processo de aquecimento ou laranja escuro quando a reação alcalinizar. Os aminoácidos que detecta são principalmente tirosina e triptofano.
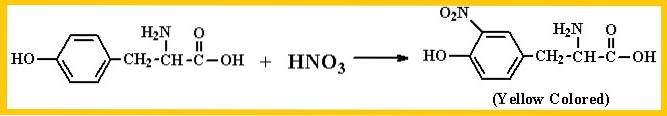
No caso da fenilalanina, embora seja um aminoácido aromático, o núcleo de benzeno deste aminoácido é difícil de ser nitrado em uma reação simples, portanto, ele emitirá uma reação negativa ou positiva fraca.
Em geral, o teste da xantoproteína pode ser complementado com o teste Hopkins-Cole, que é usado para identificar especificamente o triptofano. Se o teste da xantoproteína for positivo e o teste de Hopkins-Cole for negativo, a presença de triptofano naquela solução é descartada, apontando para a presença principalmente de tirosina. Da mesma forma, também pode ser complementado com a reação de Millon para a detecção de tirosina, entre outras coisas..
Esta reação também pode ser usada em amostras de sangue, plasma ou soro dessalbuminado para o diagnóstico de uremia ou insuficiência renal. Nesse caso, o que se busca é a detecção de substâncias tóxicas (fenólicas e indol) produzidas a partir da putrefação intestinal..
Essas substâncias possuem o grupo benzeno e, portanto, dão uma reação de xantoproteína positiva, embora a substância reagente não seja um aminoácido nem uma proteína..
Processar
- Reação de xantoproteína para detecção de aminoácidos com grupos aromáticos
Coloque 1 ml da amostra de teste em um tubo de teste limpo e seco.
-Adicione 0,5 ml de ácido nítrico concentrado.
-Incubar a mistura em banho-maria a 70 ° C por 2 minutos. Prepare previamente o banho-maria na temperatura mencionada.
-Ao retirar o tubo do banho-maria, é possível observar que a solução ficou leitosa e adquiriu uma certa cor branco-amarelada..
-A solução é resfriada jogando água fria na base do tubo..
-A preparação é tornada alcalina pela adição lenta (gota a gota) de uma solução de hidróxido de sódio a 40% até que haja uma mudança de cor.
-Se o teste for positivo, um anel laranja escuro se formará na interface dos líquidos..
-Se a reação for negativa, não haverá formação de cor.
- Reação de xantoproteína para detectar substâncias fenólicas e indol no sangue
-Dispensar 5 cc de ácido tricloroacético 20% em 5 cc de sangue venoso, plasma ou soro, sendo este último o mais indicado. Misture bem e filtre.
-2 ml do filtrado são retirados e misturados com 0,5 ml de ácido nítrico. Em seguida, é aquecido até à fervura, para isso o tubo é colocado diretamente sobre a chama do isqueiro por 30 segundos. Arrefece-se com água e adiciona-se 1,5 de cloreto de sódio a 33%..
É interpretado da seguinte forma:
-Resultado negativo: cor amarelada.
-Resultado positivo (+) amarelo limão.
-(++) amarelo dourado.
-(+++) amarelo escuro a marrom
Também pode ser interpretado usando uma escala colorimétrica de Autenrieth referencial, consistindo em várias concentrações de dicromato de potássio. Este é preparado em diluições de 10 em 10 a partir de uma solução estoque de 0,03874%. Cada tubo representa uma porcentagem.
Escalas de interpretação
Existem duas escalas de interpretação chamadas antigas e modernas. Os valores normais são:
Tabela antiga: entre 75 a 85%
Mesa moderna: entre 15 a 25%
Se a cor do tubo de ensaio estiver no meio de dois tubos padrão, uma média é feita entre as duas medições.
A solução padrão de dicromato de potássio é preparada como segue: 7,9 ml de dicromato de potássio 10 N são medidos e completados em um balão volumétrico para 100 ml. Para as diluições, siga as instruções na tabela colorimétrica de Autenrieth..

Usar
O uso da reação das xantoproteínas faz parte de um conjunto de testes bioquímicos que ajudam a conhecer a composição química de alguma substância desconhecida. Este teste contribui para a análise química a detecção de proteínas que contenham grupos benzênicos em sua estrutura..
Essa reação é amplamente utilizada por pesquisadores em vários estudos de substâncias de interesse..
Nesse sentido, Vásquez-Jorge e colaboradores utilizaram essa e outras reações para investigar o conteúdo protéico de fluidos extraídos da ostra de mangue. (Crassostrea rhizophorae).
Da mesma forma, Rojas et al (2009) usaram uma série de testes, incluindo a reação de xantoproteína, para analisar glicomacropeptídeos em precipitados de soro de ricota..
Por outro lado, a reação da xantoproteína de Becher foi modificada por Volhard para ser utilizada para outros fins. Nesse caso, para a detecção de substâncias fenólicas e indol que podem subir muito mais cedo (semanas ou meses) antes que os níveis de uréia e nitrogênio residual no sangue aumentem..
Esses resíduos tóxicos são formados a partir da putrefação intestinal de alimentos.
Essas substâncias se acumulam no sangue quando não são eliminadas corretamente; portanto, um teste de xantoproteína positivo pode prever o início precoce de insuficiência renal adequada ou um estado de uremia..
Dependendo da intensidade da cor, você pode determinar o quão avançada ela é. Neste caso, o teste é quantitativo.
Em pessoas saudáveis, este teste dá uma leve cor amarela, correspondendo aos níveis normais de triptofano e tirosina que podem estar no sangue.
Já em pacientes renais a reação das xantoproteínas é fortemente positiva devido à presença das seguintes substâncias: fenol, indol, paracresol, oxiácidos aromáticos, entre outros.
Precauções
Este teste deve ser realizado por profissionais treinados. Todos os regulamentos de biossegurança devem ser considerados, uma vez que os reagentes utilizados são ácidos e bases corrosivas..
Se por acaso caírem algumas gotas de ácido nítrico na pele ou nas unhas, amarelarão, pois ambas as estruturas contêm proteínas. Além disso, na pele e nas membranas mucosas, causa queimaduras graves.
Se ocorrer contato com a pele, o protocolo a seguir deve ser lavar a área imediatamente com água e sabão por aproximadamente 20 minutos..
Se respingar nos olhos, deve-se lavar com bastante água doce, procurando manter os olhos abertos..
Referências
- "Reação de xantoproteína" Wikipédia, a enciclopédia livre. 2 de setembro de 2019, 17:49 UTC. 21 de outubro de 2019, 20:31 wikipedia.org/
- Vásquez-Jorge Y, Guerra-Molina L, Quintana-Tamayo J, Ramírez-Arzuaga J, Fernando-Ballesteros R, Vásquez-Jorge Y. Caracterização físico-química e teor de proteínas de extratos fluidos de ostra de mangue (Crassostrea rhizophorae). Revolução cubana da química, 2014; 26 (1): 66-74. Disponível em Redalyc.
- Rojas E, Valbuena E, Torres G, García A, Piñero M, Galindo L. Isolamento e desempenho de GMP por precipitação de soro de leite com ácido tricloroacético. Cient. (Maracaibo) 2009; 19 (3): 295-302. Disponível em: ve.scielo.
- Reação de Vásquez A. Xanthoprotein. Revista clínica espanhola. 1949; 35 (5): 326-327. Disponível em: Elsevier
- Reações de Gálvez I, Gárate O. Becher e Andrewes em cirurgia urinária. Serviço de Urologia do Hospital Espanhol. Jornal argentino de urologia 395-404



Ainda sem comentários