
Terceira lei das fórmulas da termodinâmica, equações, exemplos
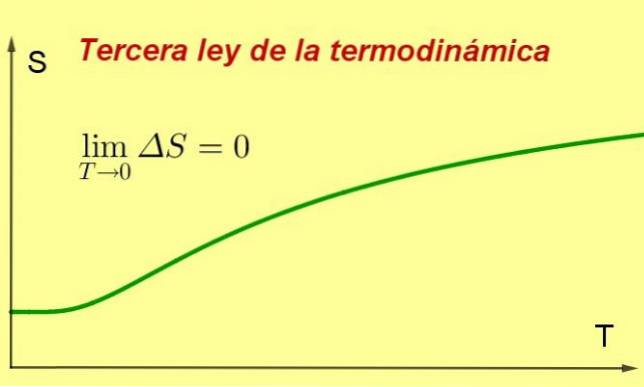
O Terceira lei da termodinâmica afirma que a entropia de um sistema termodinâmico fechado em equilíbrio tende a ser mínima e constante, à medida que sua temperatura se aproxima de 0 kelvin.
Este valor de entropia será independente das variáveis do sistema (pressão ou campo magnético aplicado, entre outros). O que acontece é que à medida que a temperatura está mais próxima de 0 K, os processos no sistema param e como a entropia é uma medida de agitação interna, ela necessariamente cai.
Índice do artigo
- 1 Conceitos anteriores
- 1.1 Sistema termodinâmico
- 1.2 Sistemas isolados, fechados ou abertos
- 1.3 Macroestados e microestados
- 2 Fórmulas e equações
- 2.1 Cálculo da entropia absoluta de uma substância
- 3 aplicativos
- 3.1 Entropia de um sistema em baixa temperatura
- 3.2 Entropia residual
- 4 exemplos
- 4.1 Exemplo 1: zero absoluto e indeterminação de Heisenberg
- 4.2 Exemplo 2: Superfluidez e o estranho caso de hélio-4
- 5 exercícios resolvidos
- 5.1 - Exercício 1
- 5.2 - Exercício 2
- 6 referências
Conceitos anteriores
Para entender o escopo da terceira lei da termodinâmica, relevante em temperaturas muito baixas, é necessário revisar os seguintes conceitos:
Sistema termodinâmico
Geralmente se refere a um gás, um líquido ou um sólido. O que não faz parte do sistema é chamado meio Ambiente. O sistema termodinâmico mais comum é o gás ideal, que consiste em N partículas (átomos) que interagem apenas por meio de colisões elásticas.
Sistemas isolados, fechados ou abertos
Sistemas isolados não são permitidos em qualquer troca com o meio ambiente. Os sistemas fechados não trocam matéria com o meio ambiente, mas trocam calor. Finalmente, os sistemas abertos podem trocar matéria e calor com o meio ambiente..
Macroestados e microestados
O macroestado de um sistema é o conjunto de valores que suas variáveis possuem: pressão, temperatura, volume, número de moles, entropia e energia interna. Já o microestado - no caso de um gás ideal - é dado pela posição e momento de cada uma das N partículas que o compõem, em um dado instante..
Muitos microestados podem resultar no mesmo macroestado. Em um gás à temperatura ambiente, o número de microestados possíveis é imenso, pois o número de partículas que o compõem, as diferentes posições e as diferentes energias que podem adotar é muito grande..
Fórmulas e equações
A entropia, como dissemos, é uma variável macroscópica termodinâmica que mede o grau de desordem molecular do sistema. O grau de desordem de um sistema é maior à medida que o número de microestados possíveis é maior.
Este conceito é necessário para formular a terceira lei da termodinâmica na forma matemática. Seja S a entropia do sistema, então:

Entropia é uma variável de estado macroscópica que está diretamente relacionada ao número de microestados possíveis de um sistema, através da seguinte fórmula:
S = k ln (W)
Na equação acima: S representa entropia, C o número de possíveis microestados do sistema e k é a constante de Boltzmann (k = 1,38 x 10-2,3 J / K) Ou seja, a entropia de um sistema é k vezes o logaritmo natural do número de microestados possíveis.
Cálculo da entropia absoluta de uma substância
É possível definir a entropia absoluta de uma substância pura a partir da definição da variação da entropia:

δQ = n. cp .dT
Aqui, cp é o calor específico molar eno número de moles. A dependência do calor específico molar com a temperatura é um dado obtido experimentalmente e conhecido para muitas substâncias puras..
De acordo com a terceira lei sobre substâncias puras:


Formulários
Na vida cotidiana, a terceira lei da termodinâmica tem poucas aplicações, exatamente o oposto da primeira e da segunda leis. É porque é um princípio que se refere ao que acontece em um sistema quando se aproxima de 0 absoluto, uma rara faixa de temperatura.
Na verdade, atingir 0 ou −273,15 ° C absolutos é impossível (ver exemplo 1 abaixo). No entanto, a terceira lei se aplica ao estudar a resposta de materiais em temperaturas muito baixas.
Graças a isso, importantes avanços surgiram na Física da matéria condensada, tais como:
-Superfluidez (ver exemplo 2 abaixo)
-Supercondutividade
-Técnicas de resfriamento a laser
-Condensado de Bose-Einstein
-Gases superfluidos Fermi.

Em temperaturas extremamente baixas, a diminuição da entropia permite o surgimento de fenômenos quânticos interessantes. Portanto, vamos ver o que acontece com a entropia de um sistema em temperatura muito baixa.
Entropia de um sistema em baixa temperatura
Quando você tem uma substância cristalina perfeita, sua entropia mínima é exatamente zero, pois é um sistema altamente ordenado. Em temperaturas próximas de 0 absoluto, a matéria está em um estado condensado (líquido ou sólido) e as vibrações no cristal são mínimas.
Alguns autores consideram uma declaração alternativa da terceira lei da termodinâmica o seguinte:
"Se a matéria se condensa para formar um cristal perfeito, quando a temperatura tende para o zero absoluto, a entropia tende para exatamente zero".
Vamos esclarecer alguns aspectos da declaração anterior:
- Um cristal perfeito é aquele em que cada molécula é idêntica e em que a estrutura molecular se repete de forma idêntica em sua totalidade..
- Conforme a temperatura se aproxima do zero absoluto, a vibração atômica diminui quase completamente.
Então o cristal forma uma única configuração ou possível microestado, ou seja, W = 1, e, portanto, a entropia é igual a zero:
S = k ln (1) = 0
Mas nem sempre um material resfriado próximo ao zero absoluto forma um cristal, muito menos esse cristal é perfeito. Isso só acontece se o processo de resfriamento for muito lento e reversível..
Caso contrário, fatores como impurezas presentes no vidro tornariam possível a existência de outros microestados. Portanto, W> 1 e a entropia seria maior que 0.
Entropia residual
Se o resfriamento for abrupto, durante ele o sistema passa por uma sucessão de estados de desequilíbrio, que levam à vitrificação do material. Nesse caso, não se produz uma estrutura cristalina ordenada, mas um sólido amorfo, cuja estrutura é semelhante à de um líquido..
Nesse caso, o valor mínimo de entropia na vizinhança do zero absoluto não é zero, uma vez que o número de microestados é consideravelmente maior do que 1. A diferença entre esta entropia e a entropia nula do estado cristalino perfeito é conhecida como o entropia residual.
A explicação é que abaixo de um determinado limiar de temperatura, o sistema não tem outra opção a não ser ocupar os microestados de menor energia, que, por serem quantizados, constituem um número fixo.
Eles cuidarão de manter a entropia constante, mesmo quando a temperatura continuar caindo para o zero absoluto..
Exemplos
Exemplo 1: zero absoluto e indeterminação de Heisenberg
O princípio de indeterminação de Heisenberg estabelece que a incerteza na posição e no momento de uma partícula, por exemplo nos átomos de uma rede de cristal, não são independentes entre si, mas seguem a seguinte desigualdade:
Δx ⋅ Δp ≥ h
Onde h é a constante de Planck. Ou seja, a incerteza na posição multiplicada pela incerteza no momento (massa vezes velocidade) é maior ou igual à constante de Planck, cujo valor é muito pequeno, mas não zero: h = 6,63 x 10-3. 4 J s.
E o que o princípio da incerteza tem a ver com a terceira lei da termodinâmica? Se a posição dos átomos na estrutura do cristal é fixa e precisa (Δx = 0), então a velocidade desses átomos pode assumir qualquer valor entre 0 e infinito. Isso é contradito pelo fato de que, no zero absoluto, todo o movimento de agitação térmica cessa..
Reciprocamente, se assumirmos que na temperatura de zero absoluto, toda a agitação cessa e o momento de cada átomo na rede é exatamente zero (Δp = 0), então o princípio da incerteza de Heisenberg implicaria que a indeterminação nas posições de cada átomo seria infinita, ou seja, eles podem estar em qualquer posição.
Como consequência da afirmação anterior, o número de microestados tenderia ao infinito e a entropia também teria um valor indeterminado.
Exemplo 2: Superfluidez e o estranho caso de hélio-4
Na superfluidez, que ocorre em temperaturas muito baixas, a matéria perde o atrito interno entre suas moléculas, denominado viscosidade. Nesse caso, o fluido poderia circular sem atrito para sempre, mas o problema é que nessas temperaturas quase nada é líquido, exceto o hélio..
O hélio e o hélio 4 (seu isótopo mais abundante) constituem um caso único, pois à pressão atmosférica e em temperaturas próximas do zero absoluto, o hélio permanece líquido..
Quando o hélio-4 é submetido a uma temperatura abaixo de 2,2 K à pressão atmosférica, torna-se um superfluido. Esta descoberta ocorreu em 1911 em Leyden pelo físico holandês Heike Kamerlingh Onnes (1853-1926).
O átomo de hélio-4 é um bóson. Os bósons, ao contrário dos férmions, são partículas que podem ocupar o mesmo estado quântico. Portanto, os bósons não cumprem o princípio de exclusão de Pauli.
Então, todos os átomos de hélio-4 a temperaturas abaixo de 2,2 K ocupam o mesmo estado quântico e, portanto, há apenas um microestado possível, o que implica que o superfluido hélio-4 tem S = 0.
Exercícios resolvidos
- Exercício 1
Vamos considerar um caso simples que consiste em um sistema composto de apenas três partículas que possuem três níveis de energia. Para este sistema simples:
a) Determine o número de microestados possíveis para três faixas de temperatura:
-Alto
-Metade
-Baixo
b) Determine por meio da equação de Boltzmann a entropia nas diferentes faixas de temperatura.
c) Discuta os resultados e explique se eles contradizem ou não a terceira lei da termodinâmica..
Solução para
Na escala molecular e atômica, as energias que um sistema pode adotar são quantizadas, o que significa que só podem assumir determinados valores discretos. Além disso, quando as temperaturas são tão baixas, as partículas que compõem o sistema só têm a possibilidade de ocupar os níveis de energia mais baixos..
Alta temperatura
Se o sistema tiver uma temperatura T relativamente alta, então as partículas terão energia suficiente para ocupar quaisquer níveis disponíveis, dando origem a 10 microestados possíveis, que aparecem na figura a seguir:
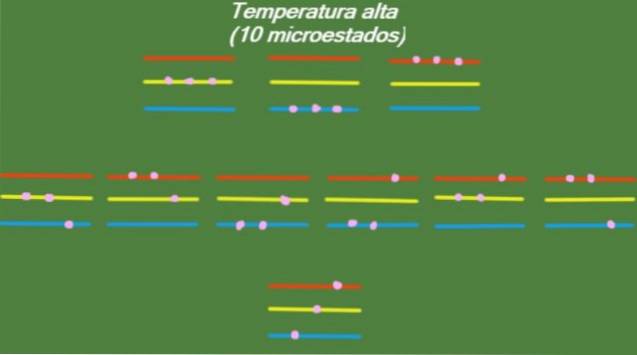
Temperatura média
No caso em que o sistema possui uma temperatura intermediária, então as partículas que o compõem não possuem energia suficiente para ocupar o nível de energia mais alto. Os possíveis microestados são ilustrados na figura:
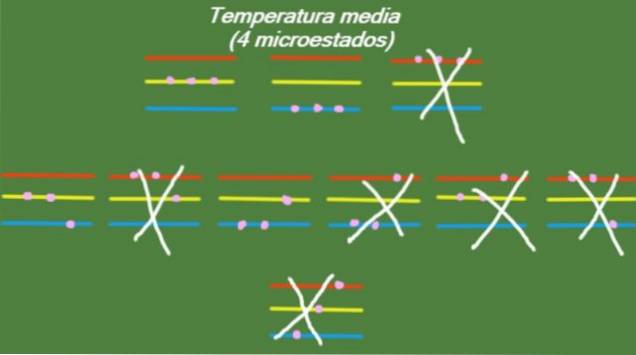
Temperatura baixa
Se a temperatura continuar caindo em nosso sistema idealizado de três partículas e três níveis de energia, então as partículas terão tão pouca energia que só serão capazes de ocupar o nível mais baixo. Neste caso, apenas 1 possível microestado permanece, conforme mostrado na figura 6:
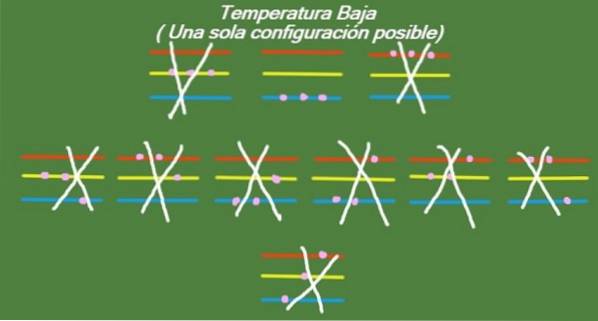
Solução b
Uma vez que o número de microestados em cada faixa de temperatura é conhecido, podemos agora usar a equação de Boltzmann dada acima para encontrar a entropia em cada caso.
S = k ln (10) = 2,30 x k = 3,18 x 10-2,3 J / K (Alta temperatura)
S = k ln (4) = 1,38 x k = 1,92 x 10-2,3 J / K (Temperatura média)
E finalmente:
S = k ln (1) = 0 (Temperatura baixa)
Solução c
Primeiro, notamos que a entropia diminui conforme a temperatura cai, como esperado. Mas, para os valores de temperatura mais baixos, um valor limite é alcançado, a partir do qual o estado básico do sistema é alcançado..
Mesmo quando a temperatura está o mais próxima possível do zero absoluto, não há estados de energia mais baixos disponíveis. Então a entropia mantém seu valor mínimo constante, que em nosso exemplo é S = 0.
Este exercício ilustra, no nível do microestado de um sistema, a razão pela qual a terceira lei da termodinâmica é válida..
- Exercício 2
Motivo se a seguinte afirmação for verdadeira ou falsa:
"A entropia de um sistema à temperatura zero absoluto é exatamente zero".
Justifique sua resposta e descreva alguns exemplos.
Solução
A resposta é: falsa.
Em primeiro lugar, o 0 absoluto da temperatura não pode ser alcançado porque violaria o princípio da incerteza de Heisenberg e a terceira lei da termodinâmica..
É muito importante notar que a terceira lei não diz o que acontece no 0 absoluto, mas sim quando a temperatura está infinitamente próxima do 0 absoluto. A diferença é sutil, mas significativa.
Nem a terceira lei afirma que, quando a temperatura assume um valor arbitrariamente próximo do zero absoluto, a entropia tende a zero. Isso só ocorreria no caso analisado anteriormente: o cristal perfeito, que é uma idealização.
Muitos sistemas em escala microscópica, ou seja, em escala quântica, têm seu nível básico de energia degenerar, o que significa a existência de várias configurações no nível de energia mais baixo.
Isso significa que, nesses sistemas, a entropia nunca seria exatamente zero. Nem a entropia seria exatamente zero em sistemas que vitrificam quando a temperatura tende a zero absoluto. Neste caso, o entropia residual antes visto.
Isso se deve ao fato de suas moléculas ficarem “presas” antes de atingirem os menores níveis de energia disponíveis, o que aumenta consideravelmente o número de microestados possíveis, impossibilitando que a entropia seja exatamente zero..
Referências
- Cengel, Y. 2012. Thermodynamics. 7ª Edição. McGraw Hill. 347.
- Laboratório de Propulsão a Jato. O lugar mais legal do universo. Obtido em: coldatomlab.jpl.nasa.gov.
- González, A. Entropia e espontaneidade. Recuperado de: geocities.ws
- Quora. Qual é o uso prático da terceira lei da termodinâmica? Recuperado de: quora.com
- Química Geral. Terceiro princípio da termodinâmica. Recuperado de: corinto.pucp.edu.pe
- Terceira lei da termodinâmica. Recuperado de: youtube.com
- Wikipedia. Entropia residual. Recuperado de: en.wikipedia.com
- Wikipedia. Terceira lei da termodinâmica. Recuperado de: en.wikipedia.com



Ainda sem comentários